四羧基苯基卟啉銅敏化P25納米二氧化鈦(CuTCPP/P25)的研究制備方法
P25處理:將商業P25粉末溶于蒸餾水中,于150℃水熱處理10小時,冷卻至室溫,離心分離沉淀,蒸餾水洗滌,在80℃過夜干燥,得到白色粉末, 標記為P25m。
5,10,15,20-四(4-羧基苯基)卟啉(TCPP)的制備:取6.08g(40.5mmol)的4-甲酰基苯甲酸和2.8g(40.5 mmol)重蒸吡咯加入120ml丙酸,加熱回流2小時。隨后將反應后混合物冷卻至室溫,加入150ml甲醇,同時冰浴冷卻攪拌0.5小時。離心分離得到沉淀,用甲醇和加熱的蒸餾水洗滌數次直至濾液澄清。將得到的紫色粉末在80℃的烘箱中干燥12小時,制得TCPP。
CuTCPP的制備:將TCPP (0.261g, 0.33mmol)和CuCl2?2H2O (0.31g, 1.82 mmol)在DMF中回流5小時,冷卻至室溫,得到紅色溶液,沉淀離心并用蒸餾水洗滌直到濾液澄清,真空干燥,得到紅色固體即為銅(Ⅱ)四羧基苯基卟啉(CuTCPP)。
CuTCPP/P25m催化劑制備:將相應質量比的P25m和CuTCPP加入到乙醇溶液中,在90℃下回流5小時;再將反應混合液冷卻、離心,并用乙醇洗滌直至濾液澄清,以除去過量的CuTCPP;然后在80℃下干燥,制得CuTCPP/P25m,CuTCPP/P25制備方法同上。
銅(Ⅱ)四羧基苯基卟啉敏化P25納米二氧化鈦性能測試:
將商業P25通過水熱處理的方法,得到表面羥基數量增加P25m。然后將P25和P25m分別與不同質量的CuTCPP在乙醇溶液中回流,得到不同質量比的CuTCPP/P25和CuTCPP/P25m。CuTCPP與P25 和P25m通過化學鍵聯接,該催化劑被用于光催化CO2還原,表現出**的還原產CH4性能。性能測試表明,在300W 氙燈下,CuTCPP/P25m催化活性較純P25m,CO2還原性能明顯提高。其中0.5%CuTCPP/P25m還原產率分別為19.39 CH4 μmol/g/h、2.68 CO μmol/g/h,其中較純P25m催化產出CH4的量提高了約46倍。
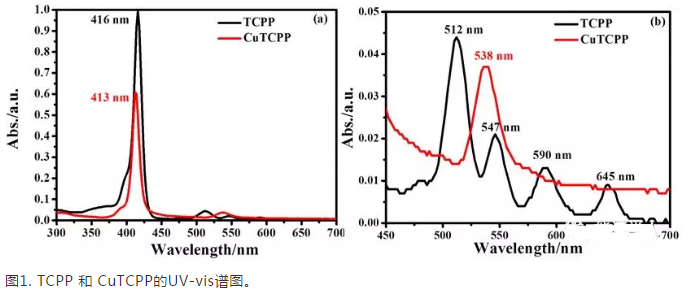
TCPP 和 CuTCPP的UV-vis譜圖中分別出現不同吸收吸收強度的吸收峰S帶(強)和Q帶(弱),這是由于卟啉S帶的摩爾消光系數遠大于Q帶的摩爾消光系數,因此吸收強度不同。與TCPP相比,CuTCPP的Q帶吸收峰的數量減少,在413 nm和538 nm處出現兩個新峰,這是金屬卟啉的形成的標志。由于TCPP環的四個N原子化學環境不對稱,因此Q-帶呈現4個吸收峰。與此相反,當TCPP四個N原子與金屬Cu2+離子配位后,其空間對稱性增加,N原子化學環境相同,CuTCPP的Q帶減少為1個吸收峰。
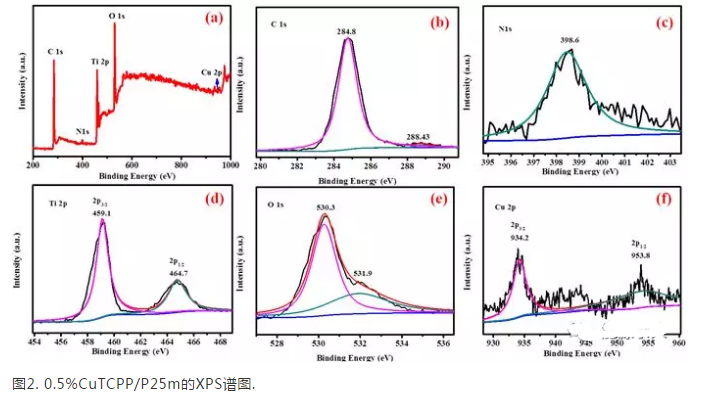
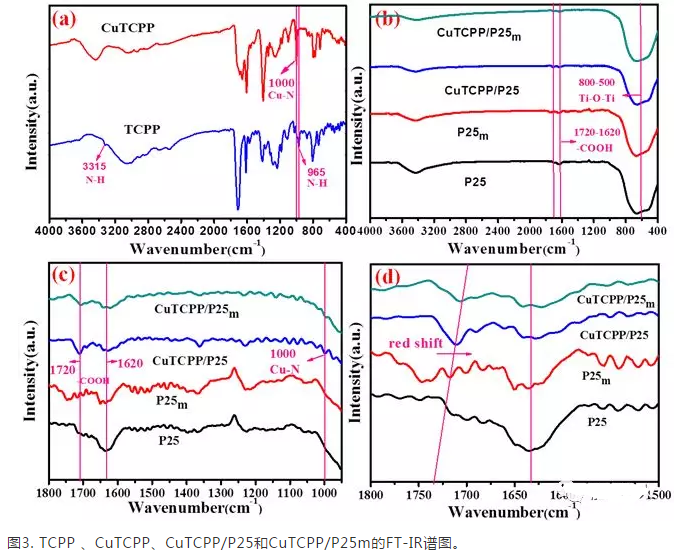
FT-IR譜圖中,TCPP 的N-H振動峰出現在3315 cm-1、965 cm-1。當形成金屬卟啉絡合物CuTCPP時, 3315 cm-1和965 cm-1附近的吸收峰消失,而在1000 cm-1附近出現新的Cu-N特征峰,這是卟啉配體與金屬離子形成絡合物的主要特征。在復合催化劑CuTCPP/P25m的FT-IR譜圖中,同時也存在CuTCPP的特征峰。
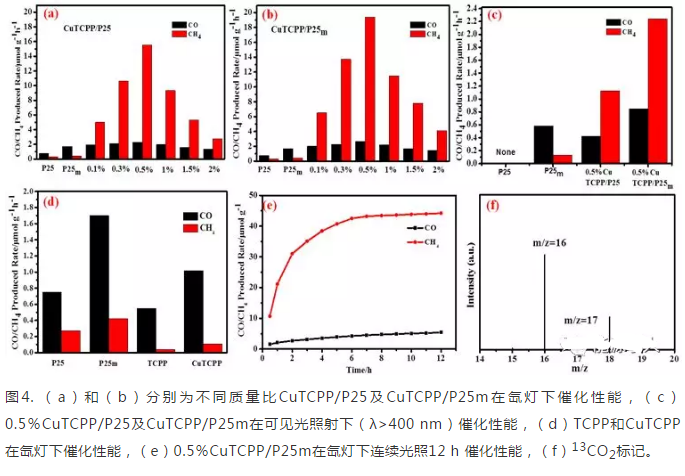
通過上述性能測試發現,同一質量比下CuTCPP/P25m的催化活性優于CuTCPP/P25,這可能是由于P25m表面增加的羥基使得吸附了更多的CuTCPP,使其催化活性增加。不同質量比條件下,0.5% CuTCPP/P25m具有催化活性,其產率分別為19.39 μmol/g/h 的CH4 以及2.68 μmol/g/h 的 CO。同時對 0.5% CuTCPP/P25m連續光照12 h發現,其依然保持催化活性。13CO2同位素追蹤實驗表明,通入的CO2是其還原過程中碳源。
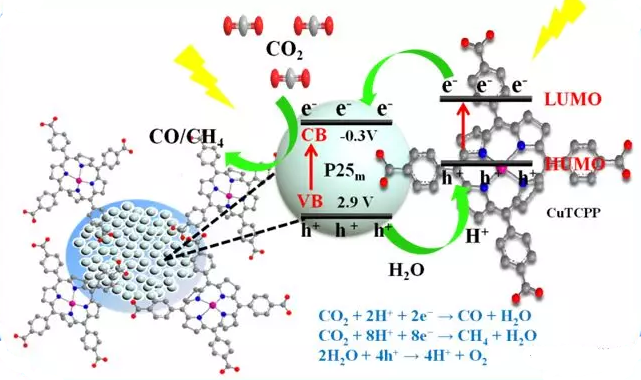
圖5. CuTCPP/P25m還原機理圖
結論:
用水熱的方法對P25m改性后,與CuTCPP回流成功制備CuTCPP/P25m催化劑。性能測試發現,該催化劑在300 W 氙燈下表現出CO2還原產CH4能力。通過進一步機理分析發現,銅(Ⅱ)四羧基苯基卟啉(CuTCPP)有助于提高P25的光吸收能力及光生電子和空穴的分離效率。此外,含有羧基的卟啉分子與P25表面羥基通過化學鍵聯接,從而提高了材料的催化活性和穩定性。




 齊岳微信公眾號
齊岳微信公眾號 官方微信
官方微信 庫存查詢
庫存查詢