一文介紹RhCl3三氯化銠作用下小分子肽與硼酸的反應活性
Rh(III)鹽參與的有機金屬生物偶聯反應:酪氨酸殘基發生金屬化形成Rh(III)/酪氨酸配合物,并同時與硼酸試劑轉金屬化引入官能化的芳基片段,該復合物又可以在強還原劑二硫蘇糖醇(DTT)作用下分解為氨基酸殘基。他們利用這種方法實現了多肽和蛋白質在水溶液介質中溫和的生物偶聯,同時還可引入其他重要的官能團,如親和基團或熒光基團。基于無機連接體的亞穩定性,偶聯產物僅在親核性的氧化還原物種存在時才會被切斷,對**的生物環境較為穩定。
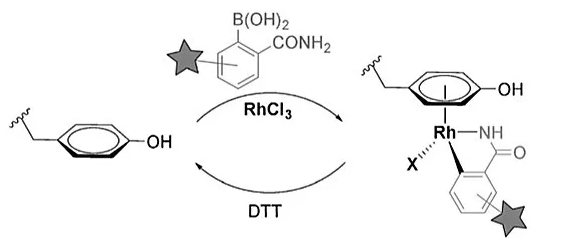
考察不同過渡金屬鹽對硼酸轉化的反應活性,以炔烴官能化的芳基硼酸對酪氨酸殘基進行修飾,使用“化學”蛋白質印跡分析的方法確定引入硼酸基團的效果。僅有兩種金屬鹽能參與配位炔烴標記的蛋白質:一種是先前報道的銅(II)鹽參與的反應,另一種涉及Rh(III)參與的過程,簡單的RhCl3鹽便可作為的金屬促進劑。
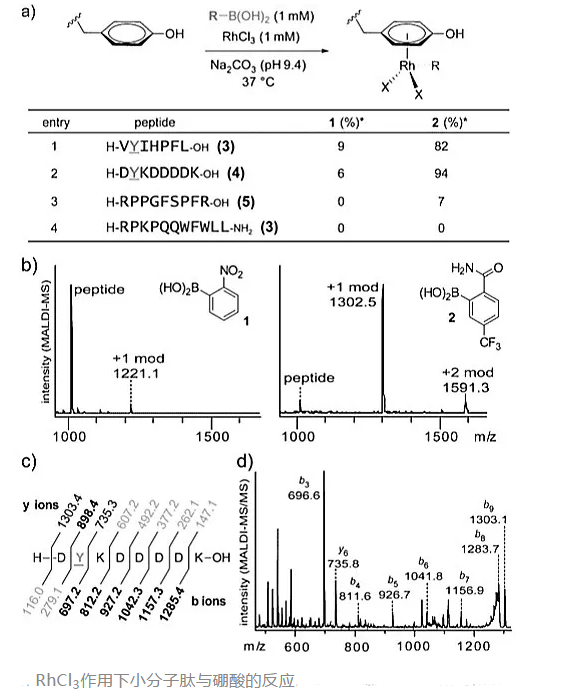
通過小分子肽設計的實驗確定了酪氨酸殘基是成功實現修飾過程的充要條件。以RhCl3對四種小分子肽進行修飾,以Na2CO3溶液作為緩沖體系,在37 ℃的反應溫度下反應18 h,鄰位含有酰胺基且間位含有三氟甲基的苯硼酸2表現出比鄰硝基苯硼酸1更好的反應活性。由于H-RPPGFSPFR-OH與H-RPKPQQWFWLL-NH2中沒有酪氨酸殘基,小分子肽未表現出明顯的反應活性。利用質譜分析考察生成產物的比例,以分子離子峰及碎片峰的信息確定了酪氨酸殘基是有機金屬修飾的位點。
以上資料來自互聯網,如有侵權,請聯系我們進行刪除
僅用于科研




 齊岳微信公眾號
齊岳微信公眾號 官方微信
官方微信 庫存查詢
庫存查詢