小分子交聯(lián)劑對(duì)于探測生物分子間的相互作用和在處理大型蛋白復(fù)合物和內(nèi)在無序蛋白時(shí)的交聯(lián)質(zhì)譜(CXMS)是非常寶貴的。現(xiàn)有的化學(xué)交聯(lián)劑只針對(duì)一小部分氨基酸殘基,限制了交聯(lián)的數(shù)量和類型,而傳統(tǒng)的光交聯(lián)劑幾乎不選擇性地針對(duì)所有殘基,使數(shù)據(jù)分析變得復(fù)雜。
設(shè)計(jì)合成了基于光保護(hù)的喹酮甲基化(PQM)的一系列交聯(lián)劑,能夠通過的Michael加成靶向9個(gè)親核殘基。除了Asp、Glu、Lys、Ser、Thr和Tyr外,PQM交聯(lián)劑還**地交聯(lián)了Gln、Arg和Asn,**,這些化學(xué)交聯(lián)劑還不能作為靶點(diǎn),用單一交聯(lián)劑**地增加了靶點(diǎn)殘基的數(shù)量。
設(shè)計(jì)了一種含NHS酯基和光保護(hù)ortho-QM(o-QM)的雙功能交聯(lián)劑NHQM。鄰硝基芐基在酚羥基上的鄰位甲基上連接了兩個(gè)氟原子,當(dāng)加入到蛋白中時(shí),NHS會(huì)很快和暴露的Lys殘基反應(yīng),將光保護(hù)的o-QM放置在相互作用蛋白的殘基旁邊,o-硝基芐基在紫外線照射下被清除,生成o-QM,并與附近的親核側(cè)鏈發(fā)生交聯(lián)。
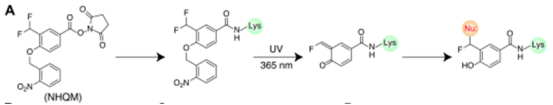
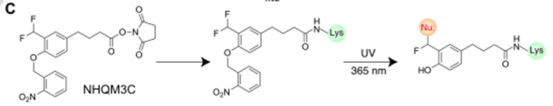
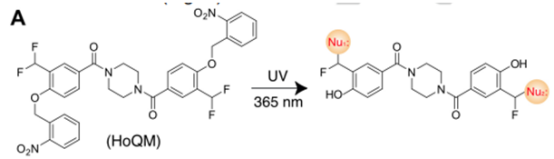
為了增加交聯(lián)劑的靈活性,還合成了NHQM3C,在NHQM的spacer 中添加了三個(gè)亞甲基。實(shí)驗(yàn)結(jié)果表明,NHQM和NHQM3C用小分子交聯(lián)劑將自然殘基的靶標(biāo)庫擴(kuò)大到9個(gè)親核殘基。為了使細(xì)胞內(nèi)**的交聯(lián)成為可能,還設(shè)計(jì)了一個(gè)具有同功能的交聯(lián)劑HoQM,在兩端都采用了光保護(hù)的o-QM。將NHS酯替換為光保護(hù)的QM可以在光激活前消除交聯(lián)劑的化學(xué)反應(yīng)性,從而使其進(jìn)入細(xì)胞而不會(huì)引起細(xì)胞毒性。此外,兩端的QM可以增加交聯(lián)類型的多樣性,因?yàn)?/span>QM與NHS酯相比會(huì)和更多的殘基反應(yīng)。
與DNA交聯(lián)的試劑仍然很少,因?yàn)榇蠖鄶?shù)交聯(lián)劑的反應(yīng)更傾向于蛋白-蛋白而不是蛋白-DNA交聯(lián)。甲醛是主要的試劑交聯(lián)試劑,但只能和在2埃以內(nèi)的蛋白發(fā)生交聯(lián)。QM能**地烷基化脫氧核苷,因此,推斷NHQM應(yīng)該能夠使蛋白質(zhì)與DNA交聯(lián),實(shí)驗(yàn)證明假設(shè)是正確的。
總之,這些PQM交聯(lián)劑的光活化和多靶點(diǎn)反應(yīng)性將大大增強(qiáng)蛋白質(zhì)-蛋白質(zhì)、蛋白質(zhì)- DNA網(wǎng)絡(luò)研究和結(jié)構(gòu)生物學(xué)研究的化學(xué)交聯(lián)基礎(chǔ)技術(shù)。
更多技術(shù)資料及其相關(guān)產(chǎn)品了解,可瀏覽官網(wǎng)首頁分欄。




 齊岳微信公眾號(hào)
齊岳微信公眾號(hào) 官方微信
官方微信 庫存查詢
庫存查詢