外泌體對細胞和動物模型的影響
室實驗僅能證明上下兩室的兩種細胞之間確實發生了物質運輸傳遞,接下來,通過外泌體跟蹤測試這些ATM分泌的外泌體是否可以被脂肪細胞吸收。從ATM細胞提取外泌體,加上PKH26標簽,添加到3T3-L1脂肪細胞培養基中,12h后,在細胞里面觀察得到紅色的帶PKH26標簽的外泌體。
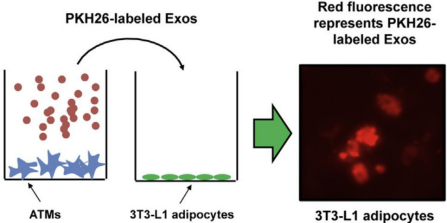
外泌體對細胞和動物模型的影響
已經證實ATM細胞分泌的外泌體能夠轉運miRNA到3T3-L1脂肪細胞,接下來可以把外泌體添加到細胞培養基或靜脈注射到動物模型,觀察表型。從肥胖小鼠ATM中提取外泌體,靜脈注射到正常小鼠中,2周后,發現小鼠的葡萄糖耐受能力、胰島素敏感性、葡萄糖輸注率(GIR)、胰島素刺激的葡萄糖代謝速率(IS-GDR)、肝臟糖產出量(HGP)和循環系統中的游離脂肪酸(FFA)都下降了,而瘦的小鼠來源的ATM-exo沒有產生影響。表明肥胖動物的ATM細胞產生含miRNA的外泌體,在體內減弱胰島素敏感性(圖1)。將上述外泌體添加到多種細胞株的培養基中,24h后可觀察得細胞胰島素敏感性下降,與動物實驗結果一致(圖2)。
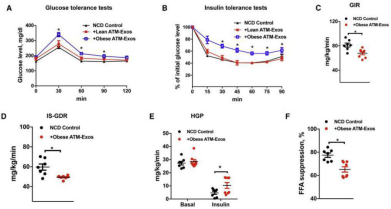
圖一
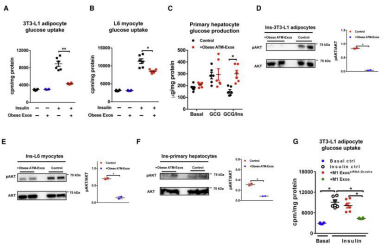
圖二
外泌體miRNA測序
已知是外泌體中的miRNA發揮了**的作用,可到底是哪些miRNA呢,可以通過高通量測序尋找其中起著關鍵作用的分子。測序樣本:瘦的ATM-exo VS 肥胖ATM-exo。測序獲得的差異表達miRNA中,miR-155曾被報道通過**PPARγ,影響脂肪細胞分化,miR-155繼續研究
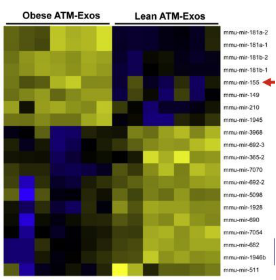
圖三
miRNA的功能
3T3-L1脂肪細胞轉染miR-155 mimic后,細胞葡萄糖吸收量減少(圖4);敲除miR-155后細胞胰島素刺激的葡萄量吸收量上升;但移植骨髓后,miR-155重新表達,使細胞的葡萄糖吸收再次減少(圖5)。
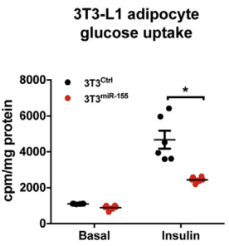
圖四
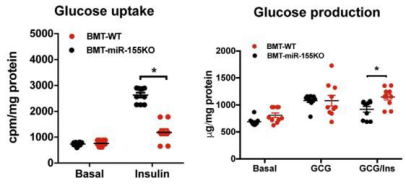
圖五
(1)脂肪組織巨噬細胞分泌的外泌體miRNA可調節體內和體外胰島素敏感性;
(2)脂肪組織巨噬細胞分泌的外泌體向胰島素靶細胞傳遞miRNA;
(3)肥胖ATM外泌體**瘦小鼠引起胰島素抵抗;
(4)瘦素ATM外泌體**肥胖小鼠改善胰島素抵抗;
(5)肥胖ATM外泌體含有miR155,可引起胰島素抵抗。
來源:本文來源網絡,版權歸相關權利人所有,如侵權,請聯系刪除。




 齊岳微信公眾號
齊岳微信公眾號 官方微信
官方微信 庫存查詢
庫存查詢